art 01.
Myelination
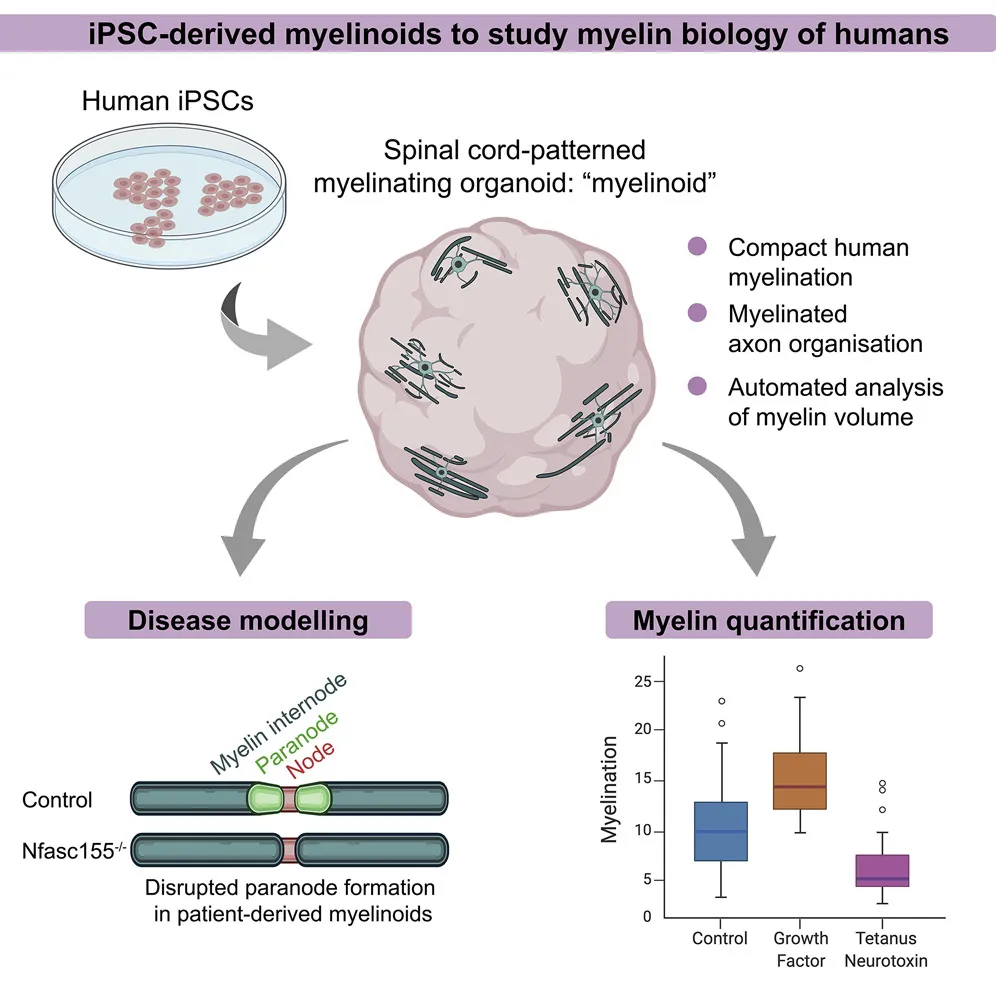
图1.整体实验设计
文章主要可以分解为两个主要部分,首先是介绍如何建立髓鞘类器官的过程,即如何从人 iPSCs 培养形成髓鞘类器官的方法和流程,其次就是如何以形成的髓鞘类器官进行评估验证,以证明其可以作为有效模型。
P
art 02.
Myelination
iPSC 衍生的髓鞘类器官的产生和表征
因为前脑类器官表现出稀疏的髓鞘形成,缺乏适当组织的有髓轴突结构,从而限制了它们在健康和疾病中人类髓鞘生理学机制评估中的应用。因此体外模拟皮质髓鞘发育特别具有挑战性。
他们的培养方法参考了以前 Livesey 等人 2016 年发表的培养少突胶质细胞的方法[4],但是为了生成人类髓鞘形成培养物,他们调整了上述方案以诱导脊髓图案的三维类器官中少突胶质细胞的成熟。简而言之,就是在用 PDGF-AA、IGF-1 和 T3 处理以诱导少突树发生之前,将双重 SMAD 抑制产生的胚状体暴露于视黄酸 (RA) 和平滑激动剂 (SAG) 以分别促进尾侧化和腹侧化。为了开始分析髓鞘形成的时间发展,类器官在 MI-0、MI-4、MI-8 和 MI-12 处用 CNP 染色, (MI 指髓鞘诱导后第几周)。具体过程和验证结果如下图所示:
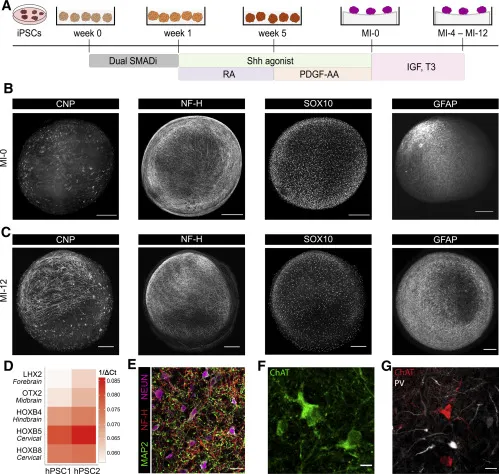
图2.实验方案时间点和部分代表性结果
(A) 生成脊髓图案类器官的方案示意图。(B) CNP +少突胶质细胞、NF-H +轴突、SOX10 +少突胶质细胞和 GFAP + MI-0 星形胶质细胞的代表性图像。(C) CNP +少突胶质细胞、NF-H +轴突、SOX10 +少突胶质细胞和 GFAP + MI-12 星形胶质细胞的代表性图像。(D) qRT-PCR 衍生的 MI-0 类器官中延髓和尾部基因表达评估的热图。(E) 分别通过 MAP2、NF-H 和 NEUN 对神经元树突、轴突和细胞体进行免疫染色。(F) ChAT +运动神经元的免疫染色。(G) ChAT 和小清蛋白 (PV) 的免疫染色显示不同神经元亚型的分化。
通过以上显微成像和 qPCR 结果可见,HOXB5 和 HOXB8 的脊髓鉴定高表达。免疫荧光分析神经亚型可见,ChAT+ 阳性的运动神经元和 PV+ ISLET1/2 阳性的中间神经元,揭示了特性区域的神经分化。
iPSC 衍生的髓鞘类器官的验证
髓鞘在单个细胞和全髓鞘水平上可预测地响应药理学线索,研究者们接下来评估了人类髓鞘形成是否可以在髓鞘内进行药理学操作,因此旨在开发工具来量化单个细胞水平和整个髓鞘内的髓鞘变化。首先,我们追踪每个细胞的单个髓鞘以评估单个少突胶质细胞形态。为了测量髓鞘形成的整体水平,他们开发了一种自动图像采集和分析方法,使用 ImageXpress 和 MetaXpress 软件,允许对髓鞘体积和轴突密度进行无偏 3D 量化如下图:
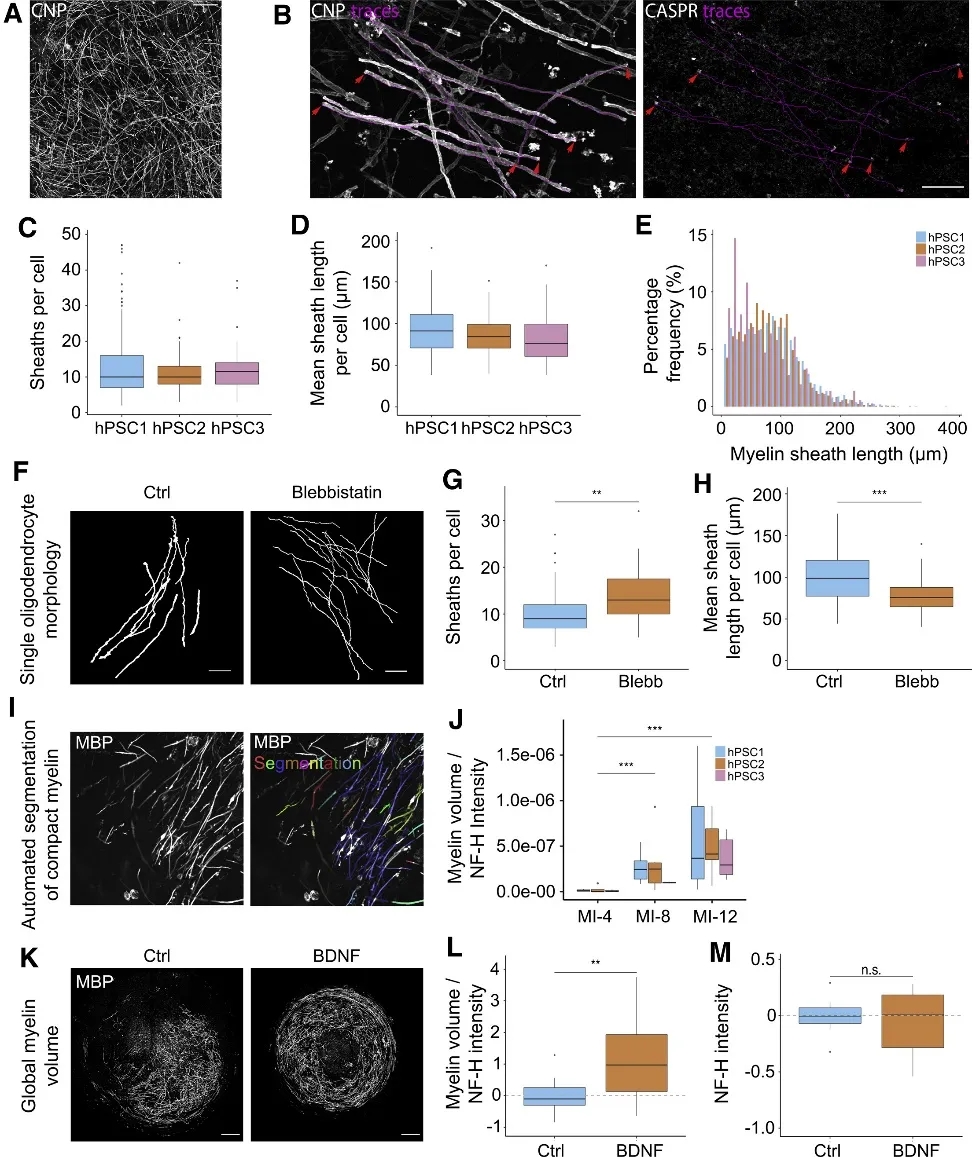
图3.图像的定量分析
(A) 用于追踪每个细胞单个髓鞘的平铺区域的代表性图像。(B) CNP +髓鞘长度的手动追踪。CASPR + PNJ(红色箭头)精确重叠手动追踪的髓鞘长度(洋红色)的远端。(C) 每个细胞的鞘数分析。(D) 每个细胞的平均鞘长度分析。(E) MI-12 时髓鞘长度的百分比频率分布。(F) Ctrl 和 blebbistatin 处理的培养物的单个细胞的骨架化 CNP +髓鞘。(G) 与 Ctrl相比,经 blebbistatin 处理的培养物中每个细胞的鞘数增加了 44.5%。(H) 与 Ctrl 相比,经布雷他汀处理的培养物中每个细胞的平均鞘长度减少了 24%。(I)自动分割 MBP +髓鞘的代表性图像。(J) 随着时间的推移,对归一化为 NF-H 强度的髓磷脂体积的自动分析显示 MI-4 和 MI-8 之间总体增加了 8 倍。(L) 髓磷脂体积归一化为 NF-H 强度的自动分析显示经 BDNF 处理的髓鞘增加了 2.09 倍。(M) NF-H 强度的自动分析显示 Ctrl 和 BDNF 处理的髓鞘样细胞之间没有变化。
通过以上结果可见,高内涵系统自动识别和定量分析的髓鞘体积 NF-H 荧光强度,随时间明显增加。并且,类器官通过 BDNF(一种以前被证明可以促进髓鞘生长的成分)处理,结果显示也能明显增加髓鞘体积,增加到差不多 2 倍。而且其体积通过 NF-H 荧光强度标准化,NF-H 荧光强度基本保持不变,来排除对轴突发育的影响。所以以上结果证明了这种利用高内涵自动 3D 体积分析的方法可以用于验证和定量髓鞘。
破伤风毒素 (TeNT) 抑制人类髓鞘形成
许多细胞和动物模型表明,少突胶质细胞调节髓鞘结构以响应神经元活动的变化, 迄今为止,没有证据表明人类髓鞘形成本身会因神经元活动的改变而发生变化。为了解决这个问题,他们试图评估是否可以通过阻断突触小泡 (SV) 释放来抑制体外人髓鞘形成。所以作者使用 Tetanus toxin (TeNT)来抑制髓鞘,应用上述髓鞘类器官为模型,和基于高内涵的自动 3D 分析方法进行定量评估,其结果如下:
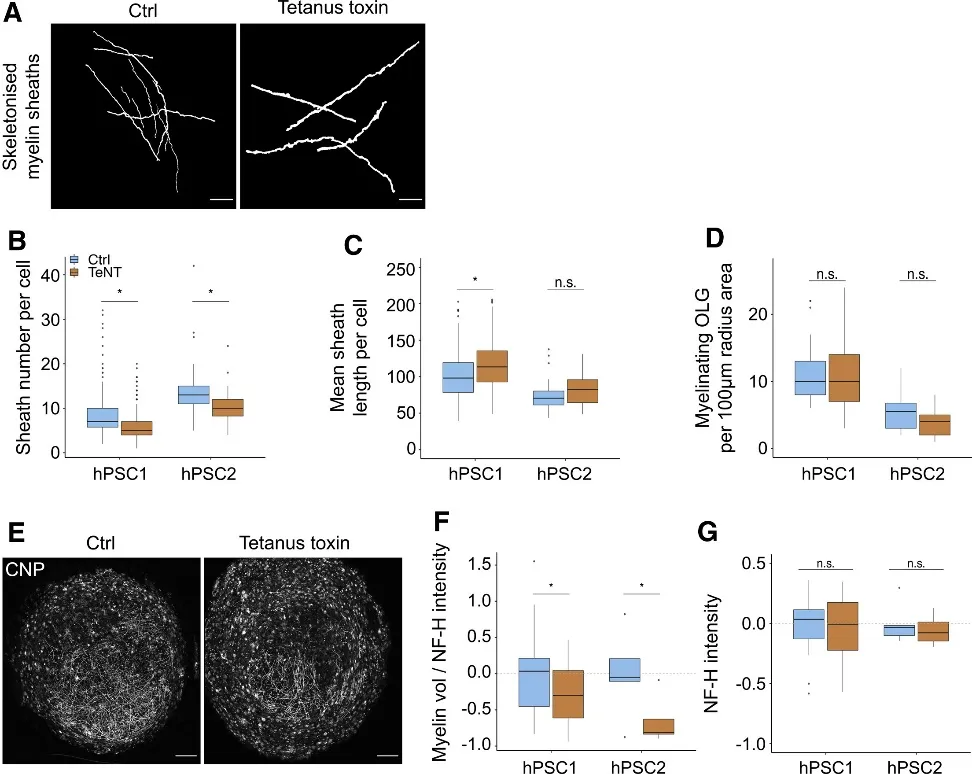
图4. 破伤风毒素处理后的图像的定量分析
(A) 来自 Ctrl 和 TeNT 处理的培养物的单个细胞的骨架化 CNP +髓鞘。(B) Ctrl 和 TeNT 处理的髓鞘内每个细胞的鞘数。在 TeNT 处理的髓鞘样细胞中,每个细胞的鞘数量总体减少了 20%(95% CI:6% 至 31%;p = 0.006);GLMM,治疗为固定效应,独特的髓鞘 ID 和细胞系为随机效应。hPSC1:减少 19%;hPSC2:减少 23%。(C) Ctrl 和 TeNT 处理的髓鞘内每个细胞的平均鞘长度。在 TeNT 处理的髓鞘样细胞中,每个细胞的平均鞘长度总体增加了 14%。(D) 最近邻分析显示 Ctrl 和 TeNT 处理的髓鞘细胞之间的少突胶质细胞密度没有变化。(F) 归一化为 NF-H 强度的髓鞘体积的自动分析表明,TeNT 处理的髓鞘总体基减少了 38%。(G) NF-H 荧光强度的自动分析。
可见,TeNT 处理可以抑制髓鞘类器官的髓鞘生成,体积降低的同时 NF-H 保持不变,可见 TeNT 对髓鞘的影响不是来源于对轴突发育的影响。
验证过程中主要仪器平台
实验所使用的主要仪器是 Imagexpress 高内涵系统,它是一种用于高通量类器官分析的自动化成像系统,可以快速、高效地获取细胞和类器官的图像和数据。

图5. Imagexpress 高内涵系统
具体实验设置如下:为了获取用于髓鞘体积自动分析的整体髓鞘,使用了 ImageXpress 显微共聚焦。对每个显微镜载玻片进行低倍率(4X)扫描,并在每个髓鞘周围绘制采集区域。在 42μm 针孔共聚焦模式下,使用 20X 复消色差物镜获取从每个采集区域 12μm 层切拍摄(1μm 的 z 轴步进),并有 10% 的重叠使拼接更加精确。

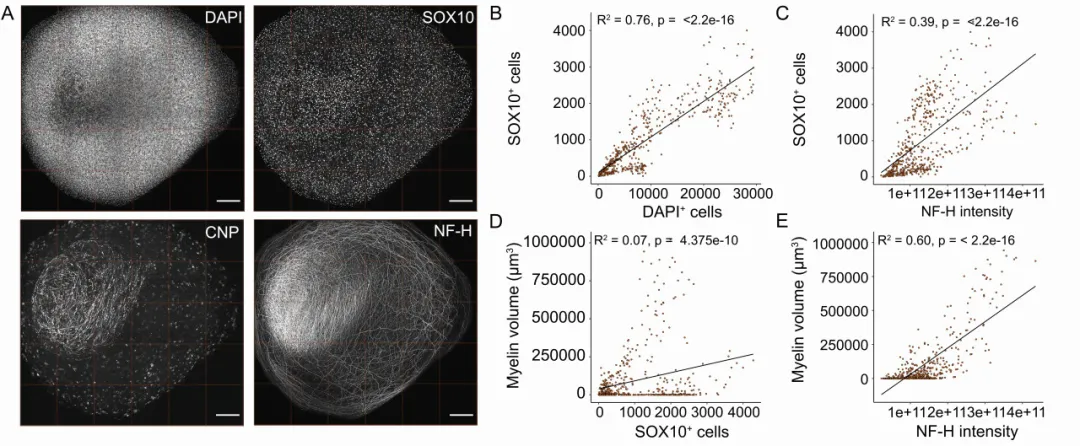
图6. Imagexpress 高内涵系统Z轴拍摄的设置
在文章的定量和统计分析章节还介绍了如何自动分析髓鞘体积。作者使用了高内涵系统配套 MetaXpress 软件中的 3D 分析功能对髓鞘体积和轴突密度进行自动化 3D 量化分析, 以获得髓鞘等结构的体积,荧光强度等 3D 定量数据,具体 3D 分析设定如下:
1.
首先通过 adaptive threshold 识别免疫荧光染色的 MBP 或 CNP。
2.
使用 Filter Mask 工具过滤掉图像中纤维长、宽、面积、形状因子不符合髓鞘形态的物体。
3.
通过 3D 连接工具将Z轴每层符合要求的髓鞘连接成 3D 的髓鞘。
4.
再通过 3D 过滤工具,过滤掉体积小于 450 立方毫米和 3D 周长小于 45 微米的物体。
实验结果如下,可见髓鞘被准确识别并产生批量可以用于分析的 3D 定量数据:
图7. Imagexpress 高内涵系统Z轴拍摄的设置
A:有代表性的 DAPI, SOX10, CNP 和 NFH 染色的同一个 MI-12 类髓鞘的图像. B-D:相关图像定量数据。
P
art 03.
Myelination
作者成功培养生成了髓鞘类器官即“类髓鞘”,并通过多种方法进行了验证。不仅如此,作者还开发了配套的基于高内涵的自动化 3D 体积定量方法,并使用破伤风毒素对此平台做了进一步的实际应用和验证,证明其可以作为相关研究甚至药物开发的潜在模型和工具。
通过这篇文章我们可以发现高内涵平台在类器官模型应用过程中的应用逐渐被应用于更广的研究领域,每篇文献所使用的高内涵功能各异,而这篇文献让我们了解到 ImageXpress 高内涵的自动化 3D 类器官体积分析功能的强大和易用性,可以成功分析髓鞘类器官这类结构复杂的类器官。
References:
[1].Bonetto G, Belin D, Káradóttir R T. Myelin: A gatekeeper of activity-dependent circuit plasticity?[J]. Science, 2021, 374(6569): eaba6905.
[2].Nave K A, Werner H B. Myelination of the nervous system: mechanisms and functions[J]. Annual review of cell and developmental biology, 2014, 30: 503-533.
[3].James O G, Selvaraj B T, Magnani D, et al. iPSC-derived myelinoids to study myelin biology of humans[J]. Developmental Cell, 2021, 56(9): 1346-1358.
[4].Livesey M R, Magnani D, Cleary E M, et al. Maturation and electrophysiological properties of human pluripotent stem cell-derived oligodendrocytes[J]. Stem cells, 2016, 34(4): 1040-1053.







 热门品牌
热门品牌





















